NOTICE
ANSM - Mis à jour le : 06/03/2024
CHOLECALCIFEROL VIATRIS 100 000 U.I, solution buvable en ampoule
Cholécalciférol
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant de prendre CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule ?
3. Comment prendre CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule ?
6. Contenu de lÂ’emballage et autres informations.
1. QUÂ’EST-CE QUE CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule ET DANS QUELS CAS EST-IL UTILISE ? <
Classe pharmacothérapeutique : vitamine D – code ATC : A11CC05
Ce médicament est indiqué dans le traitement et/ou la prophylaxie de la carence en vitamine D.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DE PRENDRE CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule ? <
Ne prenez jamais CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule :
· si vous êtes allergique à la substance active ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6 ;
· si vous présentez un excès de calcium dans le sang (hypercalcémie), un excès de calcium dans les urines (hypercalciurie), des calculs rénaux (lithiase calcique), des dépôts de calcium dans les reins (néphrocalcinose) ;
· si vous présentez une hypervitaminose D (intoxication par la vitamine D) ;
· si vous avez une maladie et/ou des troubles pouvant entraîner une hypercalcémie et/ou une hypercalciurie,
EN CAS DE DOUTE, IL EST INDISPENSABLE DE DEMANDER L'AVIS DE VOTRE MEDECIN OU DE VOTRE PHARMACIEN.
Avertissements et précautions
Adressez-vous à votre médecin, pharmacien ou votre infirmier/ère avant de prendre CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule.
Pour éviter tout surdosage, tenir compte des doses totales de vitamine D quelle qu’en soit la source, telles que des sources nutritionnelles, des compléments alimentaires de vitamine D, des médicaments contenant déjà cette vitamine ou susceptibles d’interagir avec CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule, ou en cas d'utilisation de lait supplémenté en vitamine D.
Toxicité de la vitamine D en situation d’hypervitaminose D (voir rubrique 3)
Le risque de toxicité de la vitamine D est augmenté si vous présentez une maladie et/ou des troubles entraînant un excès de calcium dans le sang et/ou dans les urines, et si vous présentez une sensibilité accrue à la vitamine D, d’origine génétique, donnant lieu à une hypervitaminose D.
Sarcoïdose
Si vous souffrez de sarcoïdose, votre médecin décidera si vous pouvez prendre ce médicament après une évaluation attentive du bénéfice de ce médicament par rapport aux risques notamment en cas de production anormale de vitamine D par votre organisme entraînant un excès de calcium dans le sang et les urines. Votre taux de calcium dans le sang et dans les urines sera étroitement surveillé. Vous ne devez pas recevoir ce médicament si vous présentez une sarcoïdose en phase active.
Insuffisance rénale
Si vous présentez une insuffisance rénale, l’effet sur les taux de calcium et de phosphate doit être surveillé. Le risque de calcification des tissus mous doit être pris en compte.
Autres médicaments et CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
En particulier, si vous prenez de la digoxine (médicament utilisé dans le traitement de l’insuffisance cardiaque et de certains troubles du rythme cardiaque) ou des diurétiques (médicaments utilisés dans le traitement de l’hypertension artérielle et de l’insuffisance cardiaque), informez votre médecin.
CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule avec des aliments et boissons
Sans objet.
En cas de besoin, ce médicament peut être pris pendant la grossesse et l'allaitement. Toutefois, cette supplémentation ne remplace pas l'administration de vitamine D chez le nouveau‑né.
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Conduite de véhicules et utilisation de machines
La vitamine D n’a aucun effet ou un effet négligeable sur l’aptitude à conduire des véhicules et à utiliser des machines.
CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule contient
Sans objet.
3. COMMENT PRENDRE CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule ? <
Carence vitaminique chez lÂ’enfant
· Prévention du rachitisme
· Sa mise en œuvre est impérative chez tous les nourrissons et les jeunes enfants, dans les conditions actuelles de vie en raison de :
o l'exposition insuffisante au soleil,
o la faible teneur des aliments en vitamine D.
Une ampoule tous les trois mois jusqu'à la 5ème année. Cette dose peut être doublée si l'enfant est peu exposé au soleil ou si sa peau est très pigmentée.
Ne pas dépasser 10 à 15 mg par an (soit 4 à 6 ampoules par an).
· Prévention de la carence en vitamine D chez le grand enfant et l'adolescent
· Une ampoule tous les trois mois en période de faible ensoleillement.
· Prévention de la carence en vitamine D chez la femme enceinte
· Une ampoule en prise unique vers le 6ème mois de la grossesse.
· Prévention de la carence en vitamine D de l'adulte et du sujet âgé
· Une ampoule tous les 3 mois.
· Traitement de la carence en vitamine D de l'adulte et du sujet âgé
· Une à deux ampoules par mois.
Ce médicament ne doit pas être utilisé chez les patients présentant une insuffisance rénale sévère (défaillance des fonctions du rein).
Mode et voie d'administration
Voie orale
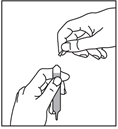
Le contenu de l'ampoule peut être administré pur ou dilué dans un peu d'eau (un léger trouble peut apparaître) ou le lait d'un biberon. L’ouverture des deux pointes de l’ampoule peut générer des débris de verre. Il est important de ne pas casser les pointes au-dessus du verre contenant le liquide. Suivre les instructions suivantes :
|
1. Tenir l’ampoule verticalement et casser la pointe supérieure puis s’assurer de l’absence de débris de verre : |
|
|
|
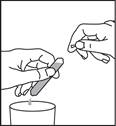
2. Retourner ensuite lÂ’ampoule au‑dessus dÂ’un verre en la tenant obliquement afin que la deuxièmepointe ne soit pas au‑dessus du verre. Casser la deuxième pointe de la même façon pour permettre au liquide de s’écouler. |
|
|
Si vous avez pris plus de CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule que vous n’auriez dû
Consultez immédiatement votre médecin ou votre pharmacien.
Un surdosage en vitamine D lors d’un traitement à court ou à long terme peut entraîner une hypervitaminose D. Cette intoxication médicamenteuse par la vitamine D peut provoquer des taux anormalement élevés de calcium dans le sang, ce qui peut finir par endommager gravement les tissus mous de l’organisme (qui ne font pas partie des os du squelette) et les reins. Ce risque est particulièrement élevé si vous recevez plusieurs sources de vitamine D et que cela ne correspond pas à vos besoins ou si vous avez une sensibilité accrue à la vitamine D, d’origine génétique, donnant lieu à une hypervitaminose D (voir rubrique 2).
Les signes cliniques d'un surdosage en vitamine D sont :
· maux de tête, fatigue, perte de l'appétit, amaigrissement, arrêt de la croissance ;
· état confus ;
· douleurs osseuses ;
· faiblesse musculaire ;
· nausées, vomissements ;
· constipation, douleurs abdominales ;
· urines abondantes, soif intense, déshydratation, soif ;
· hypertension artérielle ;
· calcul, calcification des tissus, en particulier du rein et des vaisseaux ;
· la persistance de taux de calcium élevés peut entraîner des lésions irréversibles et une calcification des tissus mous ;
· insuffisance rénale (défaillance des fonctions du rein) ;
· arythmie cardiaque (battements du cœur anormaux ou irréguliers) dans les cas graves ;
· une hypercalcémie extrême peut entraîner le coma et la mort.
Les signes biologiques d'un surdosage en vitamine D sont :
· augmentation du taux de calcium dans le sang et les urines, augmentation du taux de phosphore dans le sang et les urines, concentration sanguine basse en hormone parathyroïdienne et élevée en 25-hydroxyvitamine D.
En cas de surdosage, il faut arrêter le traitement, boire abondamment, limiter les apports en calcium (laitage) et consulter un médecin pour une prise en charge médicale.
Si vous oubliez de prendre CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez de prendre CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ? <
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) :
· allergie (réactions d’hypersensibilité) ;
· prurit, éruption cutanée, rougeur de la peau (érythème), gonflement rapide sous la peau dans des zones telles que le visage, la gorge, les bras et les jambes, qui peut mettre la vie en danger si le gonflement de la gorge bloque les voies respiratoires (angiœdème) ;
· œdème, formation de calculs de calcium (lithiase calcique) ;
· taux anormalement élevé de calcium dans le sang (hypercalcémie) ;
· taux anormalement élevé de calcium dans les urines (hypercalciurie) ;
· calculs rénaux (néphrolithiase) ;
· calcification rénale (néphrocalcinose).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule ? <
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte ou l’ampoule. La date de péremption fait référence au dernier jour de ce mois.
Conserver l’ampoule dans l’emballage extérieur.
Ne pas mettre au réfrigérateur et ne pas congeler.
Ne jetez aucun médicament au tout-à -l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE LÂ’EMBALLAGE ET AUTRES INFORMATIONS <
Ce que contient CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule <
· la substance active est :
cholécalciférol (ou vitamine D3)........................................................................................ 2,5 mg
quantité correspondant à .......................................................................................... 100 000 U.I.
pour une ampoule de 2 ml.
· Les autres composants sont :
butylhydroxytoluène, saccharine, acide sorbique, arôme naturel de citron, macrogolglycérides oléiques.
Qu’est-ce que CHOLECALCIFEROL VIATRIS 100 000 UI, solution buvable en ampoule et contenu de l’emballage extérieur <
Ce médicament se présente sous forme de solution buvable claire, jaunâtre en ampoule, avec une odeur de citron.
Boîte de 1.
Titulaire de l’autorisation de mise sur le marché <
VIATRIS SANTE
1 RUE DE TURIN
69007 LYON
Exploitant de l’autorisation de mise sur le marché <
1 RUE DE TURIN
69007 LYON
PHARMATIS
Z.A. EST N°1
60190 ESTREES-SAINT-DENIS
ou
LAPHAL INDUSTRIES
AVENUE DE PROVENCE, BP 7
13190 ALLAUCH
Noms du médicament dans les Etats membres de l'Espace Economique Européen <
Sans objet.
La dernière date à laquelle cette notice a été révisée est : <
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).