NOTICE
ANSM - Mis à jour le : 30/01/2024
REANUTRIFLEX OMEGA E, émulsion pour perfusion
Acides aminés, Glucose, Lipides, Electrolytes
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez dautres questions, interrogez votre médecin, ou votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à dautres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, ou votre pharmacien ou votre infirmier/ère. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que REANUTRIFLEX OMEGA E, émulsion pour perfusion et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser REANUTRIFLEX OMEGA E, émulsion pour perfusion ?
3. Comment utiliser REANUTRIFLEX OMEGA E, émulsion pour perfusion ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver REANUTRIFLEX OMEGA E, émulsion pour perfusion ?
6. Contenu de lemballage et autres informations.
1. QUEST-CE QUE REANUTRIFLEX OMEGA E ET DANS QUELS CAS EST-IL UTILISE ? <
REANUTRIFLEX OMEGA E contient des liquides et des substances appelées acides aminés, électrolytes et acides gras, qui sont essentiels pour permettre à lorganisme de se développer et de se rétablir. Le produit contient également des calories sous la forme de glucides et de lipides.
REANUTRIFLEX OMEGA E est administrée à des adultes, à des adolescents et à des enfants âgés de plus de 2 ans.
REANUTRIFLEX OMEGA E vous est administré lorsque vous êtes dans lincapacité de vous alimenter normalement. Ce peut être le cas dans de nombreuses situations, par exemple lorsque vous récupérez dune intervention chirurgicale, de blessures ou de brûlures ou lorsque vous ne pouvez pas absorber les aliments par lintermédiaire de votre estomac et de vos intestins.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DUTILISER REANUTRIFLEX OMEGA E ? <
Nutilisez jamais REANUTRIFLEX OMEGA E :
· si vous êtes allergique aux substances actives, aux ufs, à larachide, au soja, au poisson ou à lun des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· Ce médicament ne doit pas être administré aux nouveau-nés, aux nourrissons et aux jeunes enfants âgés de moins de deux ans.
Par ailleurs, vous ne devez pas utiliser REANUTRIFLEX OMEGA E si vous souffrez de lun des troubles suivants :
· problèmes de circulation sanguine constituant une menace pour votre pronostic vital comme ceux pouvant se produire si vous êtes en état de collapsus ou de choc
· crise cardiaque ou accident vasculaire cérébral
· trouble sévère de la coagulation du sang, risque de saignement (coagulopathie sévère, terrain hémorragique en voie daggravation)
· obstruction de vaisseaux sanguins par des caillots de sang ou de graisse (embolie)
· insuffisance hépatique sévère
· altération de la sécrétion biliaire (cholestase intrahépatique)
· insuffisance rénale sévère en labsence de traitement de substitution rénale
· perturbations de la composition en sels de votre organisme
· présence deau en quantité insuffisante ou excessive dans votre corps
· présence deau dans vos poumons (dème pulmonaire)
· insuffisance cardiaque sévère
· certains troubles du métabolisme, tels que
o quantité excessive de lipides (graisses) dans le sang
o anomalies congénitales du métabolisme des acides aminés
o taux de sucre dans le sang anormalement élevé dont le contrôle nécessite ladministration de plus de 6 unités dinsuline par heure
o anomalies du métabolisme pouvant survenir après des opérations ou des blessures
o coma dorigine indéterminée
o apport en oxygène insuffisant dans les tissus
o taux dacide anormalement élevé dans le sang
Avertissements et précautions
Adressez-vous à votre médecin, à votre pharmacien ou à votre infirmier/ère avant dutiliser REANUTRIFLEX OMEGA E.
Veuillez informer votre médecin si :
· vous avez des problèmes au cur, au foie ou aux reins ;
· vous souffrez de certains types de troubles métaboliques tels quun diabète, des taux anormaux de graisses dans le sang et des altérations de la composition en liquides et en sels ou de léquilibre acido-basique de votre organisme.
Les signes précoces dune réaction allergique (tels que fièvre, frissons, éruption cutanée ou essoufflement) seront étroitement surveillés lorsque vous recevrez ce médicament.
Le personnel infirmier pourra également prendre les mesures nécessaires pour sassurer que les besoins de votre corps en liquides et en électrolytes sont satisfaits. En plus de REANUTRIFLEX OMEGA E, il est possible que lon vous administre des nutriments (éléments nutritionnels) supplémentaires afin que vos besoins soient entièrement couverts.
Enfants
Autres médicaments et REANUTRIFLEX OMEGA E
Informez votre médecin, votre pharmacien ou votre infirmier/ère si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
REANUTRIFLEX OMEGA E peut interagir avec dautres médicaments. Informez votre médecin, votre pharmacien ou votre infirmier/ère si vous prenez ou recevez lun des médicaments suivants :
· insuline,
· héparine,
· médicaments utilisés pour prévenir la formation indésirable de caillots de sang, comme la warfarine ou les autres dérivés coumariniques,
· médicaments favorisant le débit urinaire (diurétiques),
· médicaments utilisés pour traiter lhypertension artérielle ou des problèmes cardiaques (inhibiteurs de lenzyme de conversion [IEC] et antagonistes des récepteurs de langiotensine II),
· médicaments utilisés lors des greffes dorganes, comme la ciclosporine et le tacrolimus,
· médicaments utilisés pour traiter linflammation (corticostéroïdes),
· préparations hormonales affectant léquilibre hydrique (hormone adrénocorticotrope, appelée ACTH).
REANUTRIFLEX OMEGA E avec des aliments
Sans objet.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament. Si vous êtes enceinte, vous recevrez ce médicament uniquement si votre médecin ou pharmacien juge quil est absolument indispensable à votre rétablissement. Il nexiste pas de données disponibles sur lutilisation de REANUTRIFLEX OMEGA E chez la femme enceinte.
Lallaitement est déconseillé chez les mères recevant une nutrition parentérale.
Conduite de véhicules et utilisation de machines
Ce médicament est normalement administré à des patients immobilisés, à lhôpital ou dans une clinique par exemple, ce qui exclut la possibilité de conduire des véhicules ou dutiliser des machines. Cependant, le médicament en lui-même na aucune influence sur laptitude à conduire des véhicules et à utiliser des machines.
REANUTRIFLEX OMEGA E contient du sodium
Ce médicament contient 1,244 mg de sodium (composant principal du sel de cuisine/table) par ml. Cela équivaut à 0,062% de lapport alimentaire quotidien maximal recommandé de sodium pour un adulte.
La dose journalière maximale recommandée de ce médicament contient 3 048 mg de sodium (présent dans le sel de table). Cela équivaut à 152 % de lapport alimentaire quotidien maximal recommandé de sodium pour un adulte.
Parlez-en à votre médecin ou votre pharmacien si vous avez besoin dune poche ou plus dune poche quotidiennement pendant une période prolongée, surtout si vous devez suivre un régime à faible teneur en sel (sodium).
3. COMMENT UTILISER REANUTRIFLEX OMEGA E ? <
Veillez à toujours utiliser ce médicament en suivant exactement les indications de votre médecin ou pharmacien. Vérifiez auprès de votre médecin ou pharmacien en cas de doute.
Ce médicament vous sera administré en perfusion intraveineuse (goutte à goutte), cest-à-dire directement dans une veine à laide dun petit tube. Ce médicament doit être administré uniquement dans une de vos grosses veines (centrales).
La durée de perfusion recommandée pour une poche de nutrition parentérale est de 24 h maximum.
Votre médecin ou pharmacien déterminera la quantité de ce médicament dont vous avez besoin et pendant combien de temps vous devrez être traité(e) par ce médicament.
Utilisation chez les enfants
Ce médicament ne doit pas être donné aux nouveau-nés, aux nourrissons et aux jeunes enfants âgés de moins de deux ans.
Votre médecin déterminera la quantité de ce médicament dont votre enfant aura besoin et pendant combien de temps votre enfant devra être traité par ce médicament.
Si vous avez utilisé plus de REANUTRIFLEX OMEGA E que vous nauriez dû :
Si vous avez reçu une quantité excessive de ce médicament, vous pourriez présenter ce que lon appelle un « syndrome de surcharge » et les symptômes suivants :
· excès de liquides et troubles électrolytiques
· présence deau dans vos poumons (dème pulmonaire)
· pertes dacides aminés dans les urines et perturbation de léquilibre en acides aminés
· vomissements, nausées
· frissons
· taux de sucre élevé dans le sang
· présence de glucose dans les urines
· déficit hydrique
· concentration du sang beaucoup plus importante que la normale (hyperosmolalité)
· altération ou perte de conscience due à un taux de sucre extrêmement élevé dans le sang
· augmentation du volume du foie (hépatomégalie) avec ou sans jaunisse (ictère)
· augmentation du volume de la rate (splénomégalie)
· dépôts de graisse dans les organes internes
· anomalies des constantes de la fonction hépatique
· diminution du nombre de globules rouges (anémie)
· diminution du nombre de globules blancs (leucopénie)
· diminution du nombre de plaquettes (thrombopénie)
· augmentation des globules rouges immatures (réticulocytose)
· destruction des cellules sanguines (hémolyse)
· hémorragie ou tendance aux saignements
· trouble de la coagulation du sang (mise en évidence par des modifications des temps de saignement, temps de coagulation, temps de prothrombine, etc )
· fièvre
· taux de graisses élevés dans le sang
· perte de conscience
Si lun de ces symptômes apparaît, la perfusion doit être immédiatement interrompue.
Si vous avez dautres questions sur lutilisation de ce médicament, demander plus dinformations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ? <
Les effets indésirables suivants peuvent être graves. Si lun des effets indésirables suivants survient, prévenez immédiatement votre médecin ; il arrêtera de vous donner ce médicament :
Rare (pouvant affecter jusquà 1 personne sur 1 000) :
· réactions allergiques, avec par exemple réactions cutanées, essoufflement, gonflement des lèvres, de la bouche et de la gorge, difficultés à respirer
Les autres effets indésirables comprennent :
Peu fréquent (pouvant affecter jusquà 1 personne sur 100) :
· sensation nauséeuse, vomissements, perte dappétit
Rare (pouvant affecter jusquà 1 personne sur 1 000) :
· tendance accrue du sang à former des caillots
· coloration bleuâtre de la peau
· essoufflement
· maux de tête
· bouffées de chaleur
· rougeur de la peau (érythème)
· transpiration
· frissons
· sensation de froid
· élévation de la température corporelle
· somnolence
· douleur au niveau de la poitrine, du dos, des os ou de la région lombaire
· diminution ou augmentation de la pression artérielle
Très rare (pouvant affecter jusquà 1 personne sur 10 000) :
· taux de graisses ou de sucre anormalement élevés dans le sang
· taux élevés de substances acides dans le sang
· un excès de lipides peut entraîner un syndrome de surcharge graisseuse. Pour plus dinformations à ce sujet, veuillez-vous reporter au paragraphe « Si vous avez utilisé plus de REANUTRIFLEX OMEGA E que vous nauriez dû » dans la rubrique 3. Les symptômes disparaissent normalement après larrêt de la perfusion.
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) :
· diminution du nombre de globules blancs (leucopénie)
· diminution du nombre de plaquettes (thrombopénie)
· altération de la sécrétion de la bile (cholestase)
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou, votre pharmacien ou à votre infirmier/ère. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr.
En signalant les effets indésirables, vous contribuez à fournir davantage dinformations sur la sécurité du médicament.
5. COMMENT CONSERVER REANUTRIFLEX OMEGA E ? <
Tenir ce médicament hors de la vue et de la portée des enfants.
À conserver à une température ne dépassant pas +25 °C.
Ne pas congeler. En cas de congélation accidentelle, jeter la poche.
Nutilisez pas ce médicament après la date de péremption indiquée sur létiquette. La date de péremption fait référence au dernier jour de ce mois.
Conserver la poche dans lemballage extérieur, à l'abri de la lumière.
Ne jetez aucun médicament au tout-à-légout ou avec les ordures ménagères. Demandez à votre pharmacien déliminer les médicaments que vous nutilisez plus. Ces mesures contribueront à protéger lenvironnement.
6. CONTENU DE LEMBALLAGE ET AUTRES INFORMATIONS <
Ce que contient REANUTRIFLEX OMEGA E <
· Les substances actives contenues dans le mélange prêt à lemploi sont :
|
Compartiment supérieur |
Dans 1 000 mL |
Poche de 625 mL |
Poche de 1 250 mL |
Poche de 1 875 mL |
|
Glucose monohydraté |
158,4 g |
99,00 g |
198,0 g |
297,0 g |
|
équivalent glucose |
144,0 g |
90,00 g |
180,0 g |
270,0 g |
|
Phosphate monosodique dihydraté |
2,496 g |
1,560 g |
3,120 g |
4,680 g |
|
Acétate de zinc dihydraté |
7,024 mg |
4,390 mg |
8,780 mg |
13,17 mg |
|
Compartiment central |
Dans 1 000 mL |
Poche de 625 mL |
Poche de 1 250 mL |
Poche de 1 875 mL |
|
Triglycérides à chaîne moyenne |
20,00 g |
12,50 g |
25,00 g |
37,50 g |
|
Huile de soja raffinée |
16,00 g |
10,00 g |
20,00 g |
30,00 g |
|
Triglycérides dacides gras oméga 3 |
4,000 g |
2,500 g |
5,000 g |
7,500 g |
|
Compartiment inférieur |
Dans 1 000 mL |
Poche de 625 mL |
Poche de 1 250 mL |
Poche de 1 875 mL |
|
Isoleucine |
3,284 g |
2,053 g |
4,105 g |
6,158 g |
|
Leucine |
4,384 g |
2,740 g |
5,480 g |
8,220 g |
|
Chlorhydrate de lysine équivalent lysine |
3,980 g |
2,488 g 1,991 g |
4,975 g 3,982 g |
7,463 g 5,973 g |
|
Méthionine |
2,736 g |
1,710 g |
3,420 g |
5,130 g |
|
Phénylalanine |
4,916 g |
3,073 g |
6,145 g |
9,218 g |
|
Thréonine |
2,540 g |
1,588 g |
3,175 g |
4,763 g |
|
Tryptophane |
0,800 g |
0,500 g |
1,000 g |
1,500 g |
|
Valine |
3,604 g |
2,253 g |
4,505 g |
6,758 g |
|
Arginine |
3,780 g |
2,363 g |
4,725 g |
7,088 g |
|
Chlorhydrate dhistidine monohydraté équivalent histidine |
2,368 g 1,753 g |
1,480 g 1,095 g |
2,960 g 2,191 g |
4,440 g 3,286 g |
|
Alanine |
6,792 g |
4,245 g |
8,490 g |
12,73 g |
|
Acide aspartique |
2,100 g |
1,313 g |
2,625 g |
3,938 g |
|
Acide glutamique |
4,908 g |
3,068 g |
6,135 g |
9,203 g |
|
Glycine |
2,312 g |
1,445 g |
2,890 g |
4,335 g |
|
Proline |
4,760 g |
2,975 g |
5,950 g |
8,925 g |
|
Sérine |
4,200 g |
2,625 g |
5,250 g |
7,875 g |
|
Hydroxyde de sodium |
1,171 g |
0,732 g |
1,464 g |
2,196 g |
|
Chlorure de sodium |
0,378 g |
0,237 g |
0,473 g |
0,710 g |
|
Acétate de sodium trihydraté |
0,250 g |
0,157 g |
0,313 g |
0,470 g |
|
Acétate de potassium |
3,689 g |
2,306 g |
4,611 g |
6,917 g |
|
Acétate de magnésium tétrahydraté |
0,910 g |
0,569 g |
1,137 g |
1,706 g |
|
Chlorure de calcium dihydraté |
0,623 g |
0,390 g |
0,779 g |
1,169 g |
|
|
||||
|
Électrolytes [mmol] |
Dans 1 000 mL |
Poche de 625 mL |
Poche de 1 250 mL |
Poche de 1 875 mL |
|
Sodium |
53,6 |
33,5 |
67 |
100,5 |
|
Potassium |
37,6 |
23,5 |
47 |
70,5 |
|
Magnésium |
4,2 |
2,65 |
5,3 |
7,95 |
|
Calcium |
4,2 |
2,65 |
5,3 |
7,95 |
|
Zinc |
0,03 |
0,02 |
0,04 |
0,06 |
|
Chlorure |
48 |
30 |
60 |
90 |
|
Acétate |
48 |
30 |
60 |
90 |
|
Phosphate |
16 |
10 |
20 |
30 |
|
|
Dans 1 000 mL |
Poche de 625 mL |
Poche de 1 250mL |
Poche de |
|
Teneur en acides aminés [g] |
56,0 |
35,0 |
70,1 |
105,1 |
|
Teneur en azote [g] |
8 |
5 |
10 |
15 |
|
Teneur en glucides [g] |
144 |
90 |
180 |
270 |
|
Teneur en lipides [g] |
40 |
25 |
50 |
75 |
|
|
Dans 1 000 mL |
Poche de 625 mL |
Poche de 1 250mL |
Poche de |
|
Valeur énergétique sous forme de lipides (kJ [kcal]) |
1 590 |
995 |
1 990 |
2 985 |
|
Valeur énergétique sous forme de glucides (kJ [kcal]) |
2 415 |
1 510 |
3 015 |
4 520 |
|
Valeur énergétique sous forme de protéines (kJ [kcal]) |
940 |
585 |
1 170 |
1 755 |
|
Valeur énergétique non protéique (kJ [kcal]) |
4 005 |
2 505 |
5 005 |
7 510 |
|
Valeur énergétique totale (kJ [kcal]) |
4 945 |
3 090 |
6 175 |
9 260 |
|
|
|
|
|
|
|
Osmolalité [mOsm/kg] |
2 115 |
2 115 |
2 115 |
2 115 |
|
Osmolarité théorique [mOsm/L] |
1 545 |
1 545 |
1 545 |
1 545 |
|
pH |
5,0 6,0 |
5,0 6,0 |
5,0 6,0 |
5,0 6,0 |
· Les autres composants sont :
acide citrique monohydraté (pour lajustement du pH), phospholipides duf pour préparations injectables , glycérol, oléate de sodium, tout-rac-α-tocophérol, hydroxyde de sodium (pour lajustement du pH) et eau pour préparations injectables.
Quest-ce que REANUTRIFLEX OMEGA E et contenu de lemballage extérieur <
REANUTRIFLEX OMEGA E est fourni dans des poches souples multicompartiments contenant :
· 625 mL (250 mL de solution dacides aminés + 125 mL démulsion lipidique + 250 mL de solution de glucose)
· 1 250 mL (500 mL de solution dacides aminés + 250 mL démulsion lipidique + 500 mL de solution de glucose)
· 1 875 mL (750 mL de solution dacides aminés + 375 mL démulsion lipidique + 750 mL de solution de glucose)
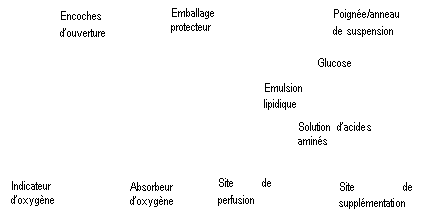
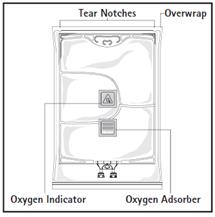
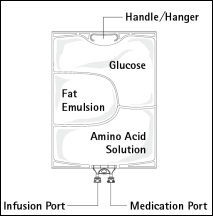
Figure A Figure B
Figure A : La poche multicompartiments est conditionnée dans un emballage protecteur. Un absorbeur doxygène et un indicateur doxygène sont placés entre la poche et lemballage protecteur ; le sachet dabsorbeur doxygène est constitué dune substance inerte et contient de lhydroxyde de fer.
Figure B : Le compartiment supérieur contient une solution de glucose, le compartiment central contient une émulsion lipidique et le compartiment inférieur contient une solution dacides aminés.
Les solutions de glucose et dacides aminés sont limpides et incolores à jaune paille. Lémulsion lipidique est dapparence blanc laiteux.
Le compartiment supérieur et le compartiment central peuvent être connectés au compartiment inférieur en ouvrant la soudure intermédiaire.
Les différents formats de conditionnement sont présentés dans des boîtes contenant cinq poches.
Présentations : 5x 625 mL, 5 x 1 250 mL et 5 x 1 875 mL
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de lautorisation de mise sur le marché <
CARL-BRAUN-STRASSE 1
34212 MELSUNGEN
ALLEMAGNE
Exploitant de lautorisation de mise sur le marché <
26 RUE ARMENGAUD
92210 SAINT-CLOUD
CARL-BRAUN-STRASSE 1
34212 MELSUNGEN
ALLEMAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen <
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen et au Royaume-Uni (Irlande du Nord) sous les noms suivants : Conformément à la réglementation en vigueur.
[à compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est : <
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de lANSM (France).
Les informations suivantes sont destinées exclusivement aux professionnels de santé :
Les médicaments de nutrition parentérale doivent être visuellement inspectés avant utilisation afin de vérifier labsence de détérioration, de changement de coloration et dinstabilité de lémulsion.
Ne pas utiliser les poches en cas de détérioration. Lemballage protecteur, le conditionnement primaire (poche) et les soudures non permanentes entre les compartiments doivent être intacts. Utiliser uniquement si les solutions dacides aminés et de glucose sont limpides et incolores à jaune paille, et si lémulsion lipidique forme un liquide homogène dapparence blanc laiteux. Ne pas utiliser si les solutions contiennent des particules.
Après mélange des trois compartiments, ne pas utiliser si lémulsion présente un changement de coloration ou des signes de séparation de phase (gouttes dhuile, film huileux). Cesser immédiatement la perfusion en cas de changement de coloration ou de signes de séparation de phase.
Avant douvrir lemballage protecteur, contrôler la couleur de lindicateur doxygène (voir la figure A). Ne pas utiliser le produit si lindicateur doxygène a viré au rose. Ne lutiliser que si lindicateur doxygène est jaune.
Préparation du mélange
Les règles dasepsie doivent être strictement respectées lors de la manipulation du produit.
Pour ouvrir : Déchirer lemballage protecteur en utilisant les encoches douverture (fig. 1). Sortir la poche de son emballage protecteur. Jeter lemballage protecteur, lindicateur doxygène et labsorbeur doxygène.
Inspecter visuellement le conditionnement primaire (poche) afin de vérifier labsence de fuite. En cas de fuite, la poche doit être éliminée car sa stérilité ne peut être garantie.
Mélange de la poche et ajout dadditifs
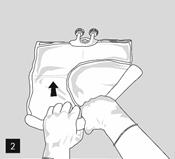
Pour ouvrir et mélanger successivement les compartiments, enrouler la poche avec les deux mains, en commençant par ouvrir la soudure pelable séparant le compartiment supérieur (glucose) du compartiment inférieur (acides aminés) (fig. 2).
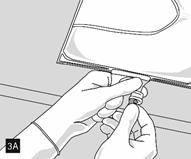
Continuer ensuite à exercer une pression de façon à ouvrir la soudure pelable séparant le compartiment central (lipides) du compartiment inférieur (fig. 3).

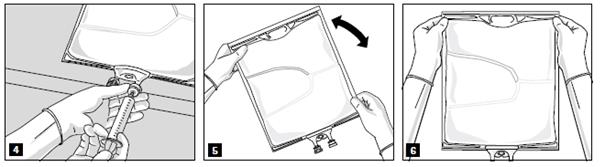
Lorsque tous les compartiments sont mélangés et après avoir retiré lopercule en aluminium (fig. 3A), les additifs compatibles peuvent être ajoutés via le site de supplémentation (fig. 4). Mélanger soigneusement le contenu de la poche (fig. 5) et inspecter visuellement le mélange (fig. 6). Le mélange est une émulsion dhuile dans leau dapparence homogène blanc laiteux. Lémulsion ne doit présenter aucun signe de séparation de phase.
REANUTRIFLEX OMEGA E peut être mélangé aux additifs suivants jusquaux limites supérieures des concentrations ou quantités maximales décrites ci-dessous après supplémentation. Les mélanges obtenus sont stables pendant 7 jours à une température comprise entre +2°C et +8°C ainsi que pendant 2 jours supplémentaires à +25°C.
· Électrolytes : prendre en compte les électrolytes déjà présents dans la poche ; la stabilité a été démontrée pour une quantité totale allant jusquà 200 mmol/L de sodium et de potassium, 9,6 mmol/L de magnésium et 6,4 mmol/L de calcium dans le mélange ternaire.
· Phosphate : la stabilité a été démontrée jusquà une concentration maximale de 20 mmol/L pour le phosphate inorganique ou jusquà une concentration maximale de 30 mmol/L pour le phosphate organique (pas les deux à la fois).
· Alanyl-glutamine : jusquà 24 g/L.
· Oligo-éléments et vitamines : la stabilité a été démontrée avec des préparations doligo-éléments et de vitamines disponibles sur le marché (par exemple Tracutil, Cernevit) conformément aux doses standards recommandées par le fabricant du micronutriment.
Des informations sur les additifs décrits ci-dessus ainsi que la durée de conservation de ces additifs peuvent être fournies sur demande par le fabricant.
Préparation de la perfusion
Lémulsion doit être systématiquement ramenée à température ambiante avant la perfusion.
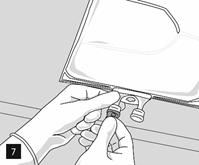
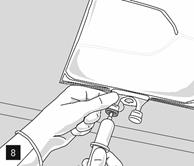
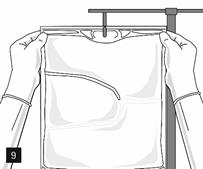
Retirer lopercule en aluminium du site de perfusion (fig. 7) et fixer la ligne de perfusion (fig. 8). Utiliser une ligne de perfusion sans prise dair ou fermer la prise dair si une ligne de perfusion avec prise dair est utilisée. Suspendre la poche sur une potence pour perfusion (fig. 9) et procéder à la perfusion selon la technique standard.
À usage unique strict. Le conditionnement et les résidus de produit inutilisés doivent être éliminés après utilisation.
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
Ne pas reconnecter des conditionnements partiellement utilisés.
Si des filtres sont utilisés, ils doivent être perméables aux lipides (taille des pores ≥ 1,2 µm).
Durée de conservation après retrait de lemballage protecteur et après mélange des contenus de la poche
La stabilité physico-chimique après reconstitution du mélange de glucose, dacides aminés et de lipides a été démontrée pendant 7 jours à une température comprise entre +2°C et +8°C ainsi que pendant 2 jours supplémentaires à +25°C.
Durée de conservation après ajout dadditifs compatibles
Dun point de vue microbiologique, le produit doit être utilisé immédiatement après ajout des additifs. Sil nest pas utilisé immédiatement après lajout des additifs, les durées et conditions de conservation avant utilisation sont sous la responsabilité de lutilisateur.
Après première ouverture (perforation du site de perfusion)
Le mélange doit être utilisé immédiatement après ouverture du conditionnement.
REANUTRIFLEX OMEGA E ne doit pas être mélangé avec dautres médicaments dont la compatibilité na pas été documentée.
REANUTRIFLEX OMEGA E ne doit pas être administré en même temps que du sang dans la même ligne de perfusion en raison du risque de pseudo-agglutination.