NOTICE
ANSM - Mis à jour le : 23/08/2023
CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule
Cholécalciférol
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez dautres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à dautres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
2. Quelles sont les informations à connaître avant de prendre CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule ?
3. Comment prendre CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule ?
6. Contenu de lemballage et autres informations.
1. QUEST-CE QUE CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule ET DANS QUELS CAS EST-IL UTILISE ? <
Classe pharmacothérapeutique : vitamine D - code ATC : A11CC05.
Ce médicament est indiqué dans le traitement et/ou la prophylaxie de la carence en vitamine D.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DE PRENDRE CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule? <
Ne prenez jamais CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule :
· si vous êtes allergique à la vitamine D ou à lun des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6,
· si vous avez un excès de calcium dans le sang ou les urines, ou des calculs rénaux.
En cas de doute, il est indispensable de demander l'avis de votre médecin ou de votre pharmacien.
Avertissements et précautions
Adressez-vous à votre médecin, pharmacien ou votre infirmier/ère avant de prendre CHOLECALCIFEROL TEVA.
Afin d'éviter tout surdosage, tenir compte des doses totales de vitamine D en cas d'association avec un traitement contenant déjà cette vitamine ou en cas d'utilisation de lait supplémenté en vitamine D.
En cas d'administration de doses fortes et répétées de vitamine D, il est nécessaire de surveiller le taux de calcium dans le sang et les urines.
En cas de doute, ne pas hésiter à demander l'avis de votre médecin ou de votre pharmacien.
Enfants et adolescents
Sans objet.
Autres médicaments et CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule avec des aliments et boissons
Sans objet.
En cas de besoin, ce médicament peut être pris pendant la grossesse et l'allaitement. Toutefois, cette supplémentation ne remplace pas l'administration de vitamine D chez le nouveau-né.
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Conduite de véhicules et utilisation de machines
Les effets sur laptitude à conduire des véhicules et à utiliser des machines nont pas été étudiés.
CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule contient
Sans objet.
3. COMMENT PRENDRE CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule? <
· Carence vitaminique chez lenfant
Prévention du rachitisme
Sa mise en uvre est impérative chez tous les nourrissons et les jeunes enfants, dans les conditions actuelles de vie en raison de :
o l'exposition insuffisante au soleil,
o la faible teneur des aliments en vitamine D.
Une ampoule tous les trois mois jusqu'à la 5ème année. Cette dose peut être doublée si l'enfant est peu exposé au soleil ou si sa peau est très pigmentée.
Ne pas dépasser 10 à 15 mg par an (soit 4 à 6 ampoules par an).
· Prévention de la carence en vitamine D chez le grand enfant et l'adolescent
Une ampoule tous les trois mois en période de faible ensoleillement.
· Prévention de la carence en vitamine D chez la femme enceinte
Une ampoule en prise unique vers le 6ème mois de la grossesse.
· Prévention de la carence en vitamine D de l'adulte et du sujet âgé
Une ampoule tous les 3 mois.
· Traitement de la carence en vitamine D de l'adulte et du sujet âgé
Une à deux ampoules par mois.
Mode et voie d'administration
Voie orale.
Le contenu de l'ampoule peut être administré pur ou dilué dans un peu d'eau (un léger trouble peut apparaître) ou le lait d'un biberon.
Louverture des deux pointes de lampoule peut générer des débris de verre. Il est important de ne pas casser les pointes au-dessus du verre contenant le liquide.
Suivre les instructions suivantes :
1 - Tenir lampoule, saisir la pointe de lampoule entre le pouce et lindex de lautre main et casser la pointe supérieure. Sassurer de labsence de débris de verre.
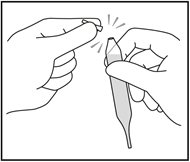
2 - Retourner ensuite lampoule au‑dessus dun verre et placer la pointe ouverte au-dessus du verre. Tenir lampoule obliquement afin que la deuxième pointe ne soit pas au‑dessus du verre. Saisir la pointe de lampoule entre le pouce et lindex et casser la deuxième pointe pour permettre au liquide de sécouler.
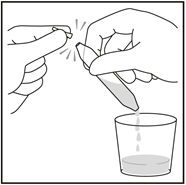
Si vous avez pris plus de CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule que vous nauriez dû
Les signes cliniques d'un surdosage sont :
· maux de tête, fatigue, perte de l'appétit, amaigrissement, arrêt de la croissance ;
· nausées, vomissements ;
· urines abondantes, soif intense, déshydratation ;
· calcul rénal, calcification des tissus, en particulier du rein et des vaisseaux ;
· insuffisance rénale (défaillance des fonctions du rein).
Les signes biologiques d'un surdosage sont :
· augmentation du taux de calcium dans le sang et les urines et augmentation du taux de phosphore dans le sang et les urines.
En cas de surdosage, il faut arrêter le traitement, boire abondamment, limiter les apports en calcium (laitage) et consulter un médecin.
Si vous oubliez de prendre CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule
Si vous arrêtez de prendre CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule
Sans objet.
Si vous avez dautres questions sur lutilisation de ce médicament, demandez plus dinformations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ? <
Les effets indésirables suivants sont rapportés très rarement et notamment en cas de surdosage (voir rubrique « Si vous avez pris plus de CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule que vous n'auriez dû ») :
· réaction d'hypersensibilité, hypercalcémie, hypercalciurie, lithiase calcique.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci sapplique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr/.
En signalant les effets indésirables, vous contribuez à fournir davantage dinformations sur la sécurité du médicament.
5. COMMENT CONSERVER CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule ? <
Tenir ce médicament hors de la vue et de la portée des enfants.
Nutilisez pas ce médicament après la date de péremption indiquée sur la boîte ou lampoule. La date de péremption fait référence au dernier jour de ce mois.
Conserver lampoule dans lemballage extérieur.
Ne pas mettre au réfrigérateur et ne pas congeler.
Ne jetez aucun médicament au tout-à-légout ou avec les ordures ménagères. Demandez à votre pharmacien déliminer les médicaments que vous nutilisez plus. Ces mesures contribueront à protéger lenvironnement.
6. CONTENU DE LEMBALLAGE ET AUTRES INFORMATIONS <
Ce que contient CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule <
· La substance active est :
Cholécalciférol (ou vitamine D3).............................................................................................. 2,5 mg
Quantité correspondant à............................................................................................... 100 000 U.I.
Pour une ampoule de 2 ml.
· Les autres composants sont :
Butylhydroxytoluène, saccharine, acide sorbique, arôme naturel de citron, macrogolglycérides oléiques.
Quest-ce que CHOLECALCIFEROL TEVA 100 000 UI, solution buvable en ampoule et contenu de lemballage extérieur <
Boîte de 1.
Titulaire de lautorisation de mise sur le marché <
SWENSWEG 5
2031 GA HAARLEM
PAYS-BAS
Exploitant de lautorisation de mise sur le marché <
100-110 ESPLANADE DU GENERAL DE GAULLE
92931 PARIS LA DEFENSE CEDEX
Z.A. EST N°1
60190 ESTREES-SAINT-DENIS
Ou
LAPHAL INDUSTRIES
AVENUE DE PROVENCE
13190 ALLAUCH
Noms du médicament dans les Etats membres de l'Espace Economique Européen <
Sans objet.
La dernière date à laquelle cette notice a été révisée est : <
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de lANSM (France).